起搏器植入植入式心脏起搏器的原理和构造
植入式人工心脏起搏器是一种很精巧的、可靠程度很高的电脉冲刺激器,是应用一定型式的起搏脉冲发生器,与特制的导线(即:起搏导管电极)连接,和起搏电极发送电脉冲刺激心脏,使激动不能或传导不好的心脏应激而起搏的医疗电子仪器。
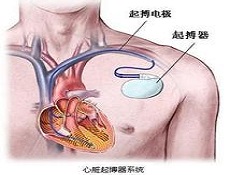
植入式人工心脏起搏器主要由以下两个部分组成:
(1)起搏导管电极:它一方面将起搏器的输出信号引向心肌进行起搏,另一方面将感知到心脏自身搏动的信号(腔内心电图ICG)反馈给起搏器以控制起搏脉冲的发放。它是心内膜电极,目前已由早期的单极发展到双极,甚至多极。作为长期起搏的导管电极必须是用生物相容性好、韧性好、抗老化、耐腐蚀的材料制成。电极导线通常采用爱尔近合金(Elgiloy)或用镍―铬―钴―钼合金丝绕成螺旋管。导线的外层绝缘材料都选用高纯硅橡胶或医用聚氨酯[3]。电极头的材料以表面活化各向彩虹低温热解碳或铂为优。
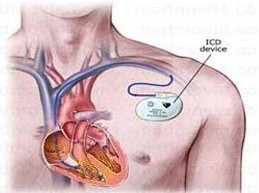
(2)起搏脉冲发生器:它由起搏电路、电池和金属外壳组成。起搏器的能源需是体积小、容量大、缓慢释放能量、密封性能好及性能可靠的电池,目前国内外植入式起搏器普遍使用锂―碘电池,使起搏器的连续使用寿命达到了10年以上。由于金属钛生物相容性好,毫无锈蚀,故目前起搏器外壳都采用钛材料拉伸成型,体型各部以较大的圆弧连接,采用激光焊接进行封装[1]。从20世纪80年代起起搏电路开始普遍采用集成电路来制造起搏器的主体电路;并将CMOS ASIC起搏芯片与电阻、电容、干簧管等电子元件一起安装在陶瓷基片上构成混合型(Hybrid)厚膜集成电路作为起搏电路的标准部件。

起搏器植入发展历史和现状
人工心脏起搏器在临床上的广泛应用,使过去药物治疗无效的严重心律失常患者得到救治,大大降低了心血管疾病的死亡率,是近代生物医学工程对人类的一项重大贡献。
1932年美国的胸外科医生Hyman发明了第一台由发条驱动的电脉冲发生器,借助两支导针穿刺心房可使停跳的心脏复跳,他命名为人工心脏起搏器(Artificial Pacemaker),从而开创了用人工心脏起搏器治疗心律失常的伟大时代。
起搏器真正用于临床是在1952年。美国医生Zoll用体外起搏器,经过胸腔刺激心脏进行人工起搏,抢救了两名濒临死亡的心脏传导阻滞病人,从而推动了起搏器在临床的应用和发展。1958年瑞典Elmgrist,1960年美国 Greatbatch分别发明和临床应用了植入式心脏起搏器。从此起搏器进入了植入式人工心脏起搏器的时代,朝着长寿命、高可靠性、轻量化、小型化和功能完善的方向发展。
早期的起搏器是固有频率型(或非同步型),只能抢救和治疗长期性房室传导阻滞、病态窦房结综合征等病症,对间歇性心动过缓不适用,不能与患者自身心律同步,会发生竞争心律而导致更严重的心律失常。为此,20世纪60年代中期先后出现了同步型起搏器,其中房同步触发型(VAT型)起搏器是专门用于房室传导阻滞,而心室按需型(VVI)是目前国内外最常用的心脏起搏器。为了使心脏起搏器与心脏自身的起搏功能相接近[1][3],70年代又相继出现了更符合房室顺序起搏的双腔起搏器(DVI),和能治疗各种心动过缓的全能型起搏器(DDD)。至此,起搏器的基本治疗功能已开发完全。
到了20世纪80年代,起搏器除了轻量化、小型化的改进外,还出现了程控和遥测的功能,利用体外程控器(Programmer)可对植入体内的起搏器进行起搏模式、频率、幅度、脉宽、感知灵敏度、不应期、A―V延迟等参数的程控调节;还可对起搏器的工作状态进行监测,将工作参数、电池消耗、心肌阻抗、病人资料乃至心腔内心电图,由起搏器发送至体外程控器中的遥测接收器进行显示[3]。90年代,起搏器又在抗心动过速和发展更适应人体活动生理变化方面取得了进展,出现了抗心动过速起搏和频率自适应起搏器(DDDR),使人工心脏起搏器成为对付致命性心律失常的有效武器。随着科学技术的发展,目前已出现了性能更高的双心室/双心房同步三腔起搏器,以及具有除颤功能的起搏器。
起搏器植入起搏器标识码
北美起搏和电生理学会(NASPE)与英国起搏和电生理组织(BPEG)以表1为识别编码。
一般情况下使用前三个识别码识别起搏器的起搏腔、感知腔和对感知(P或R波,或两者)的响应模式。供选择的第四个位置代表两种不同功能之一:程控能力或频率自适应起搏。P代表一或两种简单的程控功能;M代表多种功能程控,它包括模式、不应期、感知灵敏度和脉宽。C表明信息传递或通过一个或多个生理学变量的测量进行自适应起搏频率控制。第五位表示特殊的抗快速性心律失常特点:P代表抗快速性心律失常起搏,S表示心律复转或除颤电休克,D表示双重功能(起搏和休克)。在所有位置里,O指明类属或功能都没有提供。
起搏器植入功能类型
(1)心房按需(AAI)型
电极置于心房。起搏器按规定的周长或频率发放脉冲起搏心房,并下传激动心室,以保持心房和心室的顺序收缩。如果有自身的心房搏动,起搏器能感知自身的P波,起遏制反应,并重整脉冲发放周期,避免心房节律竞争。
(2)心室按需(VVI)型
电极置于心室。起搏器按规定的周长或频率发放脉冲起搏心室,如果有自身的心搏,起搏器能感知自身心搏的QRS波,起遏制反应,并重整脉冲发放周期,避免心律竞争。但这型起搏器只保证心室起搏节律,而不能兼顾保持心房与心室收缩的同步、顺序、协调,因而是非生理性的。
(3)双腔(DDD)起搏器
心房和心室都放置电极。如果自身心率慢于起搏器的低限频率,导致心室传导功能有障碍,则起搏器感知P波触发心室起搏(呈VDD工作方式)。如果心房(P)的自身频率过缓,但房室传导功能是好的,则起搏器起搏心房,并下传心室(呈AAI工作方式)。这种双腔起搏器的逻辑,总能保持心房和心室得到同步、顺序、协调的收缩。如果只需采用VDD工作方式,可用单导线VDD起搏器,比放置心房和心室两根导线方便得多。
(4)频率自适应(R)起搏器
本型起搏器的起搏频率能根据机体对心排血量(即对需氧量)的要求而自动调节适应,起搏频率加快,则心排血量相应增加,满足机体生理需要。目前使用的频率自适应起搏器,多数是体动型的,也有一部分是每分钟通气量型的。具有频率自适应的VVI起搏器,称为VVIR型;具有频率自适应的AAI起搏器,称为 AAIR型;具有频率自适应的DDD起搏器,称为DDDR型。以上心房按需起搏器、双腔起搏器、频率自适应起搏器都属于生理性起搏器。
(5)起搏器的程序控制功能
指埋藏在体内的起搏器,可以在体外用程序控制器改变其工作方式及工作参数。埋植起搏器后,可以根据机体的具体情况,规定一套最适合的工作方式和工作参数,使起搏器发挥较好的效能,资金节省上能而保持最长的使用寿限,有些情况下还可无创性地排除一些故障,程控功能的扩展,可使起搏器具有贮存资料、监测心律、施行电生理检查的功能。
起搏器植入房颤伴心动过缓需要安起搏器吗
心房颤动简称房颤,是最常见的持续性心律失常,房颤时心房激动的频率达300~600次/分,心跳频率往往快而且不规则,有时候可以达到100~160次/分,不仅比正常人心跳快得多,而且一定不整齐,心房失去有效的收缩功能。心动过缓是由于心脏病变引起博动异常变慢的病理现象。一般来说,如果是心动过缓,有症状,病因不可逆,就有起搏器植入的指征。
射频消融手术可以一并治愈房颤伴心动过缓吗?射频导管消融是针对快速性心律失常的。临床上的确可以看到部分房颤伴慢心室率患者消融恢复窦性心律后,并无房室传导异常,这多是由于房颤时房室连接区的隐匿性传导所致,消融消除房颤后,隐匿传导不复存在,房室传导遂恢复正常,但这部分患者在房颤伴慢心室率中占多大比例,如何检出,尚无大规模多中心的临床试验来揭示这个问题,效果并不明确。因此,房颤伴心动过缓如果伴有外周灌注不足的情况应植入起搏器。
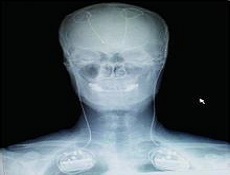
起搏器植入起搏器治扩张性心肌病
扩张型心肌病发病早期没有症状,偶尔在严重呼吸道感染或剧烈运动时感到心慌,体检可以正常,仅超声心动图检查左心室扩大。发病中期出现心力衰竭和心律失常的症状,如疲劳、乏力、胸闷、憋气、不能平卧、心慌等。发病晚期除上述症状外还可出现腹胀、食欲减退、水肿、胸水、腹水等。在发病的各个时期都有可能发生血栓栓塞和猝死,发生率分别是18%和30%。
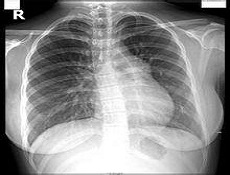
起搏器植入起搏器综合征疾病病因
其发生病因是多因素的:①房室同步收缩丧失可使心排血量降低20%~30%,如原有心功能不全者可下降50%以上;②房室瓣关闭不全引起收缩期血液反流回心房,增加心房负荷;③心房压力增高遏制了周围血管正常的收缩反射导致血压下降;④右心室起搏致使双心室收缩不同步;⑤心室心房电活动的室房逆向传导等
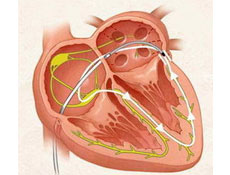
起搏器植入起搏器综合征发病机制
起搏器综合征于1960年由Mitsui等首先报道1974年,Hoss及Strait对其血流动力学及形态结构变化进行了研究。从此人们对起搏器综合征的发生机制及病理生理变化有了较深入的认识。该症的发生病因是明确的但其发病原理在于心室起搏的直接影响及异常电生理现象的影响两个方面。
双心室起搏1.心室起搏的直接影响
(1)房室非同步收缩:早在17世纪,英国生理学家Harvey就已发现心房收缩对血液循环具有重要的作用现代心脏病学已经证明心房收缩可加速心室的充盈及房室瓣的关闭这一作用称为心房的助推机制(Boosterpumpmechanism),有人用心室容积描记法研究表明在心室充盈中,心房的收缩作用可达15%-30%尤其在心功能不全时由于心室充盈的代偿功能低下需更加依赖于心房的收缩作用来维持适当的心排出量植入人工心脏起搏器作心室起搏时心房的助推机制消失,则可使心输出量明显减小。有人研究表明,可比窦性心律时减小10%-35%
(2)二尖瓣和三尖瓣反流:心室起搏下,由于房室收缩的顺序性消失,则可发生不同程度的二尖瓣和三尖瓣反流即使反流量不大也可在其他因素如房室不同步收缩的共同作用下成为起搏器综合征的促发性因素之一。
(3)心室激动过程异常:不正常的心室除极方式可致收缩的无力右室起搏表现为左束支传导阻滞的心室激动过程,可造成血流动力学方面的障碍。
(4)异常的血管反射:心室起搏后由于房室收缩不同步则心房扩张压力升高继而发生反射性周围血管阻力下降导致血压下降同时,心钠素分泌水平增加7-8倍。
2.心电生理异常的影响
起搏器综合征(1)室房逆行传导:早在20世纪60年代初进行人工心脏起搏术不久即已发现心室起搏可致室房逆行传导现象。随后许多学者对这一电生理现象进行了深入的研究结果发现病态窦房结综合征患者进行心室起搏时,60%以上的患者可有室房逆行传导。完全性房室传导阻滞患者进行心室起搏时,仍有40%的患者保持1∶1室房逆行传导。出现室房逆行传导的患者,心房不是在舒张末期加速心室的充盈,而是在房室瓣关闭的情况下有规律地将血流排至肺及腔静脉系统,从而引起右房及肺毛细血管楔嵌压的明显上升。因此,可造成严重的血流动力学障碍我们对14例起搏器综合征患者研究表明肺毛细血管楔嵌压可上升至3.3-4.0kPa(25-30mmHg),并伴明显的低心输出量而在临床上出现晕厥表现。
有人研究表明,心室起搏引起的室房逆行传导所致的血流动力学障碍远远比心房颤动及房室分离严重,是起搏器综合征的重要发病原因之一
(2)心律失常:心室起搏后可致各种心律失常如室性期前收缩,反复心律或折返性心律失常等这些心律失常者频繁、连续发生也可造成血流动力学发生障碍并导致一时性或持续性心排出量下降因此也是起搏器综合征的发生原理之一。

起搏器植入起搏器综合征疾病治疗
VVI起搏器综合征的治疗主要是防止室房逆传恢复房室收缩顺序:
1.降低起搏频率可将VVI起搏频率下调,使患者的自身节律占主导地位。起搏心律每天不大于35%,可使症状减轻
2. 改用房室顺序起搏从理论上讲,房室顺序起搏时房室顺序性收缩的同步性恢复,则心输出量增加但实际应用中发现心输出量及外周阻力均改善晚近有人发现心室起搏时发生起搏器综合征者,其外周血管阻力不增加。而无起搏器综合征者,外周血管阻力增加但两组在心室输出量方面的差别微不足道而血压具有显著性差异因此,有人建议,行心室起搏时即先测量血压,若心室起搏后血压下降25mmHg(3.33kPa),即预示发生起搏器综合征而宜行房室顺序起搏
3.消除室房逆行传导对起搏器综合征患者用抗心律失常药:如维拉帕米遏制室房逆传严重时用射频消融阻断希氏束。
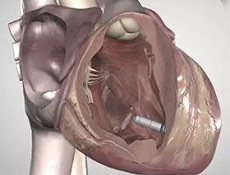
起搏器植入起搏器综合征预后预防
预后:
起搏器综合征的发生机制已十分清楚,只要为患者正确选择起搏方式和起搏器该情况是可以避免的。一旦发生起搏器综合征经正确的处理后预后较好。
预防:
在1985年以前植入的起搏器因其起搏方式无选择性,故起搏器综合征发生率较高为4.6%近10年来植入的起搏器多选用生理性起搏方式,其发生率已降至2.5%起搏器综合征是可以预防的,在安置长期性右心室起搏器前作简单的电生理和血流动力学检查寻求最适宜的起搏频率和起搏方式;避免在右心室临时起搏时有室房逆传的患者行长期性起搏尤其是病态窦房结综合征患者;尽量选用生理性起搏。对于接受VVI起搏的患者如果植入后血压即降低20mmHg以上预示着很可能发生起搏器综合征,应该植入双腔起搏器但是,双腔起搏器在左心房激动明显延迟、A-V间期程控的过长等情况下,也不排除发生起搏器综合征的可能。
起搏器植入起搏器综合征疾病诊断
建立心脏起搏器综合征诊断的主要前提是患者在安置了VVI人工心脏起搏器以后出现症状;起搏器功能正常;心脏起搏时出现血流动力学异常如血压心搏量下降静脉压、肺嵌钝压增高;自身心律出现时症状减轻或消失。
鉴别诊断
需排除神经系统疾病及患者在短期内对起搏治疗不适应而感到的不适和不能耐受。对起搏功能正常而反复发生晕厥或充血性心力衰竭的患者应进一步做心内电生理检查和血流动力学检查。如心室起搏伴有室房逆向传导和症状,而改为心房起搏或房室顺序起搏后症状明显改善或消失者;或心室起搏时动脉血压下降>20-30mmHg(2.67-4.0kPa)和右心房压升高>20mmHg(2.67kPa),同时有症状者,均应诊断为起搏器综合征
起搏器植入起搏器综合征疾病检查
实验室检查:
目前尚无相关资料
其它辅助检查:
电生理指标及血流动力学指标的检查:
1.心电生理指标心室起搏后出现室房逆行传导并出现症状,而停止起搏或改房室顺序起搏后症状消失
2.血流动力学指标心室起搏时,动脉压下降2.67kPa(20~30mmHg)以上肺毛细血管楔嵌压及右房压明显上升超过2.67kPa(20mmHg),同时出现症状。
起搏器植入生物起搏器研究状况
国内研究
在《中华医学杂志》2007年第45期,有一篇题为“自体窦房结细胞异位移植治疗缓慢型心律失常的实验研究”,此项研究为国家自然科学基金资助项目。 在这个研究项目中,有提到“窦房结”这个概念。人体心脏虽然至少有人的拳头大小,但能让这块肌肉规律跳动的指挥中心其实只有一小块地方――窦房结,这里的细胞发出信号,经过一些神经传导系统(我们在医学上称为“房室传导束支”)的传播,才使心脏肌肉细胞协调的收缩,心脏才得以发挥正常的“泵”功能,供给人体全身必须的血液。 研究人员就是充分利用了“窦房结”的起搏细胞,制作“生物起搏器”的,但在这个项目中研究人员是用犬作为实验对象,为应用于人体打下了基础。
这一课题的研究人员将16只健康成年犬分为2组(移植组和对照组),每组8只。取移植组犬的心脏窦房结组织并经过科学处理后制成存活的窦房结细胞悬液,注射到心脏另一个部位(右心室近心尖部心外膜),观察进行自体移植(移植在同一只犬身上,而不是不同只犬之间进行移植)后,这些移植细胞是否能够存活;而且,研究人员完全阻断这只犬心脏原来固有的正常的起搏系统,看看移植后的窦房结细胞是否能够发挥让心脏跳动的功能;并对移植组犬静脉注射异丙肾上腺素和阿托品这类影响心率的药物,观察其对移植后心率有无影响。
令研究人员惊喜的发现,经过移植的窦房结细胞能够在心脏的另一个部位存活;而且这些被移植的窦房结细胞能够在心室内形成新的异位起搏灶;且移植的细胞之间以及移植细胞与原有心室肌细胞之间没有排斥,都形成了有效的耦联,使其产生的电冲动信号向周围心脏肌肉扩布,从而有效驱动心室收缩;且对神经体液成分的调节有反应性。
此项研究采用自身天然的窦房结细胞进行自体移植,没有免疫排斥和肿瘤形成等问题,在生物起搏器的研发过程中,具有实用价值。但在获取和移植窦房结细胞的过程中会对细胞造成一定损伤,如何让移植后窦房结细胞的长期存活,仍有待于进一步研究证实,只有解决了这个问题,才能研制出让人类心脏能够永远稳定跳动的生物起搏器。一旦这项技术完善并成熟,应用于人体,将使心动过缓患者摆脱传统起搏器带来的不便和困绕。
国外研究
据全球优秀的医疗器材企业美敦力负责研发的高级副总裁斯蒂芬·厄斯特勒介绍,现在的心脏起搏器已经做得很小,在植入患者皮下后,患者几乎感觉不出它的存在,因此心脏起搏器的未来发展趋势并不在于它的体积大小,而在于电极的设计。起搏器的原理是通过搭在心脏上的电极来传播电刺激。但是心脏每天要跳动10多万次,而且总是在不停地扭动。在巨大的压力下,电极很有可能发生破裂,因此生产商们目前希望能开发出无电极的起搏器。
而美敦力的研发人员也正在开发可“生物起搏”的起搏器。他们希望培养出一种**,通过对其进行改造,使之分化成为能够自然跳动的细胞,然后再移植到心脏中,让它发挥起搏器的功能,这样就不再需要电池和电极了。
不过厄斯特勒指出,要想实现这一构想,还要面临两方面的挑战,其一是生物组织工程学方面的难题,即如何将其移植到人体内;另外,要获得监管部门的批准也不是一件容易的事情。厄斯特勒预计,这一技术将在20年后成熟并获得普遍应用,届时,美敦力可能不再生产现在这种机械心脏起搏器,转而生产“生物起搏器”。
此英文释义还没有添加
求医百科中的词条正文与判断内容均由用户提供,不代表求医百科立场。如果您需要解决具体问题(如法律、医学等领域),建议您咨询相关领域专业人士。
100本词条对我有帮助关于我们|招贤纳士|联系我们|用户协议|帮助中心|网站地图|内容合作|友情链接|新浪微博|下载安卓客户端
免责声明:求医网所有建议仅供用户参考。但不可代替专业医师诊断、不可代替医师处方,请谨慎参阅,本站不承担由此引起的相关责任。 Copyright © 2016 QIUYI.CN 京ICP证111012号 公安备案号11011202000697 京ICP备11039101号 互联网药品信息服务资格证书